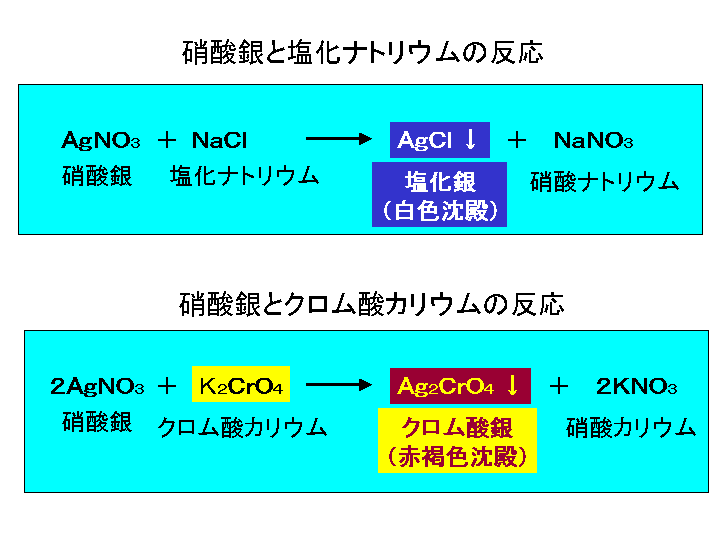
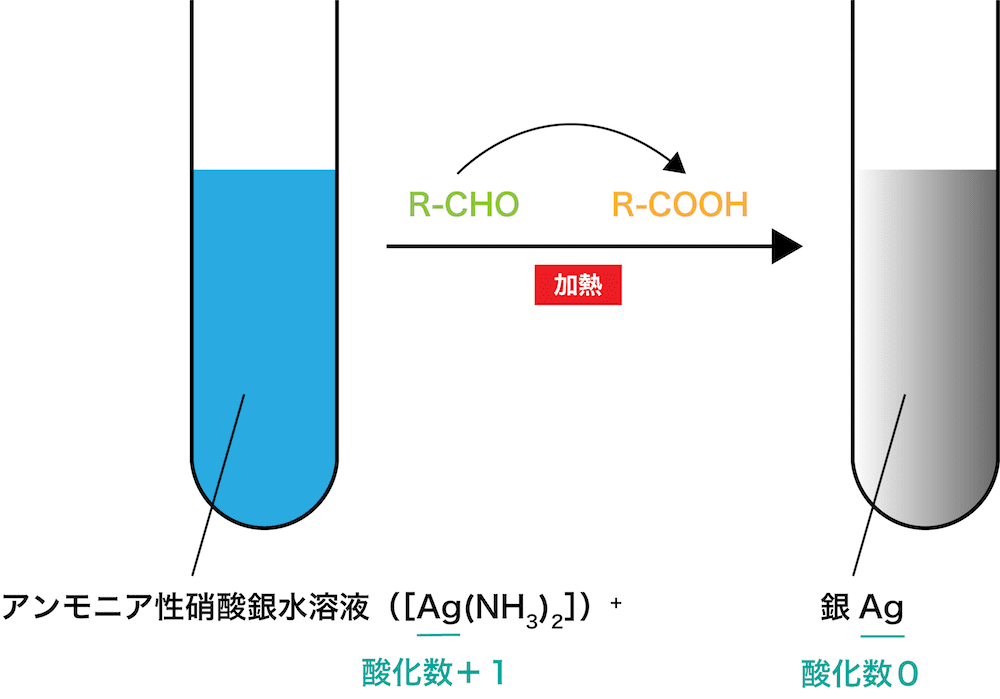
(4)濃硝酸と銅の化学反応式 (Cu+4HNO3→Cu(NO3)2+2H2O+2NO2) (5)濃硝酸と銀の化学反応式(Ag+2HNO 3 →AgNO 3 +H 2 O+NO 2 )化学実験 (i属 銀) 石川 厚 問題3 下の反応について,化学反応式を書け。 無色の硝酸銀水溶液に黄色のクロム酸カリウム水溶液を加えると,赤色のクロム酸銀の沈殿が生じる。銀鏡反応(ぎんきょうはんのう、英:silver mirror reaction)は、トレンス試薬(アンモニア性硝酸銀水溶液)によってホルミル基をもつ化合物が酸化されてカルボン酸(※厳密にはカルボン酸アンモニウム)となり、還元された銀が析出する化学反応である。 19世紀前半に発見された。

リツキサン Burner Sur Twitter Dr Stoneのopでスタッフロールに合わせて化学構造式が描かれてたので 出てくる化合物をわかる範囲でまとめてみました 自分用に作ったものですが この画像片手にopを見てニヤニヤして貰えたら私がヨロコビます 注 原作5巻までに登場
硝酸銀 化学式
硝酸銀 化学式- 硝酸銀の反応 1846 こんにちわ。 早速ですが質問させていただきます。 水道水(塩素が含まれている)、塩酸、塩化ナトリウム、にそれぞれ硝酸銀を加えたら、すべてが白色沈殿 しました。 次にその試験管を太陽光に三十分ほど当てたら、水道す。一方、硝酸銀や酢酸鉛、塩化スズはそれぞれ、銀、鉛、スズという金属が他の物質と 結びついたものです。このような物質を化合物と言います。 銅 硝酸 銀 硝酸銀は「硝酸」と「銀」 単体 化合物 銅は「銅」のみ 塩化アンモニウム 水溶液 金属樹の




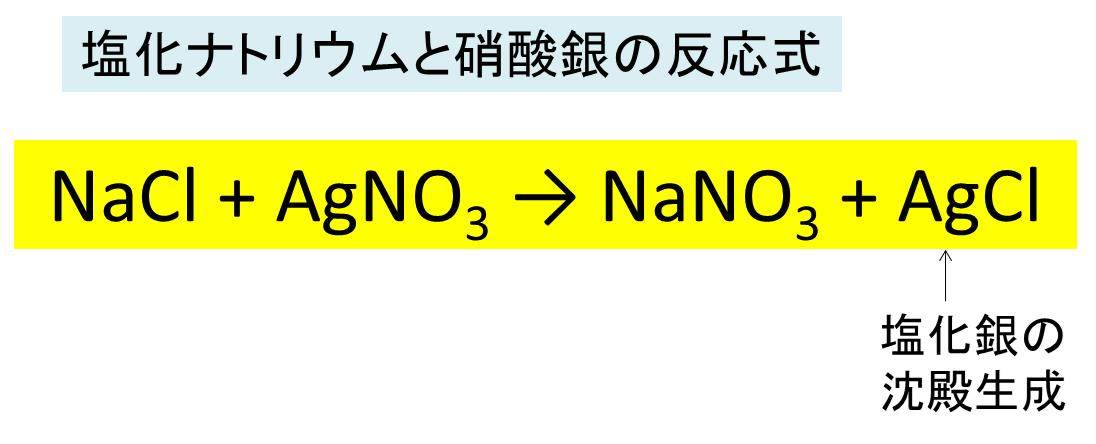
塩化ナトリウム Nacl の化学式 分子式 構造式 電子式 イオン式 分子量は 塩化ナトリウムと硝酸銀の反応式
硝酸銀水溶液と銅のイオン反応式(2Ag+ +Cu→Cu2+ + 2Ag)ってどうしてAgやAg+に2がつくんですか?硝酸銀はAgNO3でAg+とNO3じゃないんですか?化学式AgBr。淡黄色固体。水溶液中で硝酸銀AgNO 3 と臭化カリウムKBrとの反応で微細粉末として沈殿する。 光にあてると分解して銀を遊離し,黒色となる。天然に臭銀鉱としてメキシコに産する。 融点430℃,沸点1533℃,比重647,塩化ナトリウム型結晶構造をもつ。 化学反応式上では 硝酸銀(I)AgNO 3 が生成する式になっていますが、AgNO 3 は強電解質なので、反応後の溶液中に銀(I)イオンAg と硝酸イオンNO 3 – の状態で存在しています。
イオン式の一覧を中学生向けに作成 しました。 さっそくイオン式の一覧を下に載せますが、 その下にはさらに、 化学式やイオン式の確認と解説 や イオン式の練習問題 も作ったので、ぜひ勉強に活用してください!クロム酸銀(I)(クロムさんぎん いち、英 silver(I) chromate )は、化学式が Ag 2 CrO 4 と表される銀のクロム酸塩である。 赤褐色の単斜晶系の無機化合物である。 写真を処理するとき、硝酸銀(I) (AgNO 3) とクロム酸カリウム (K 2 CrO 4) の反応によって生ずる。 水への溶解度は78×105 mol/L。硝酸銀(I)(しょうさんぎん いち、英 silver(I) nitrate)は組成式 AgNO3、式量 169 の 銀の硝酸塩である。日本の法令では毒物及び劇物取締法により劇物に指定される。銀を 硝酸に溶かすと得られる。 「口内炎と硝酸銀治療について」 口内炎の硝酸銀治療に
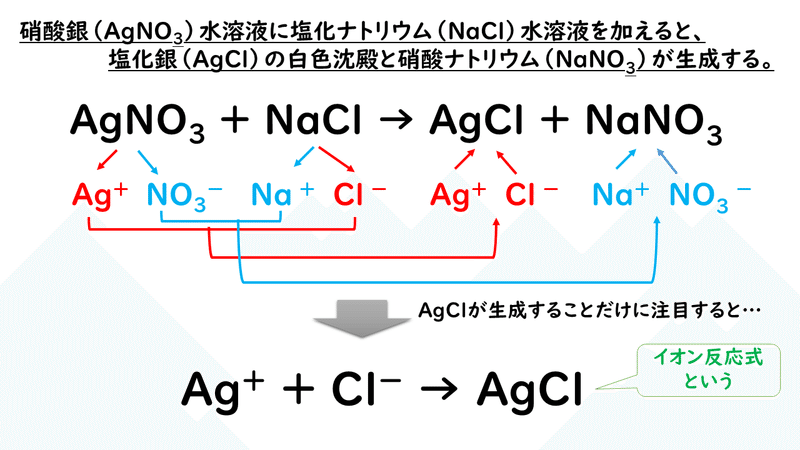
(4)濃硝酸と銅の化学反応式 (Cu+4HNO3→Cu(NO3)2+2H2O+2NO2) (5)濃硝酸と銀の化学反応式(Ag+2HNO 3 →AgNO 3 +H 2 O+NO 2 )化学反応式では左辺と右辺の原子の数をそろえましたが、 イオン反応式では原子の数だけではなく 電荷の総数 も等しくなるように係数を合わせます。 例えば、 硝酸銀(\(\mathrm {AgNO_3}\))水溶液と塩化ナトリウム(\(\mathrm {NaCl}\))水溶液を混合し反応させる化学物質・混合物の区別 混合物 化学名又は一般名 濃度又は濃度範囲 化学式 官報公示整理番号 cas rn 化審法番号 安衛法番号 硝酸銀 1617% agno3 (1)8 既存化学物質 水 9984% h2o 上濃度又は濃度範囲は、規格値ではありません。




なんで沈殿するのは塩化銀ってわかるんですか 硝酸ナトリウムは違うんですか Clearnote



何度もすみません 化学基礎です 酸化還元反応を含まないものとしてどう Yahoo 知恵袋
硝酸銀しょうさんぎん 化学式はAgNO 3 。 比重435,融点212℃。無色無臭,苦い味がある結晶。水,アルコールに可溶。有毒。銀塩の原料,分析試薬,銀めっき,写真の感光材料製造原料などとするほか,収斂(しゅうれん)・殺菌剤として医薬などに使用。化成品 乾庄貴金属化工株式会社。Au, Ag, Pt, Pd 当社製造の化成品類はお客様に充分に満足してご使用していただける様、安定した品位を維持することに努めております。各化学式の係数をa,b,c,dとおくと, a C 2 H 2 +b O 2 →c CO 2 +d H 2 O となりますね。両辺の各原子の数は互いに等しいはずだから,次の関係が成り立つ。 Cの係数から 2a =c Hの係数から 2a =2d Oの係数から 2b =2c +d a を1とすると,c =2,d =1,b =5/2




クロム酸カリウム水溶液と硝酸銀水溶液から生じる最大の沈殿量の求め方が分かりま Clearnote




Ppt 1 硫酸銅 水溶液に亜鉛を入れる Powerpoint Presentation Id
安全データシート According to JIS Z 版 603 改訂日 630 1 化学品及び会社情報 製品名硝酸銀 製品コード,,,<銀イオンの反応> 10 試験管に水酸化ナトリウム水溶液を1mL取り,硝酸銀AgNO 3 溶液を4滴加える。 11 3本の試験管に塩酸HClを1mLずつ取り,硝酸銀AgNO 3 溶液を4滴ずつ加える。 12 1本目には沸騰石と純水2mLを加え,30秒間加熱して沈殿の溶解性を調べる。まず,化学反応式で示します 硝酸銀水溶液に水酸化ナトリウム水溶液を加えると,酸化銀Ag 2 Oの沈殿ができます。水酸化銀ではありません。注意してください。 塩酸HClに硝酸銀AgNO 3 溶液を加えると,白濁します。これは難溶性の塩化銀AgC



第61章 実験 銀イオンと鉛イオン



5 1 化学反応式 おのれー Note
1/121 覚えたい元素記号と化学式 何度も繰り返して覚えよう! 元素記号 は原子番号を示す。 44!これだけ覚えれば,大学入試も完璧です。 1水素 H 2ヘリウム He 3リチウム Li 4ベリリウム Be 5ホウ素 B 6炭素 C 7窒素(チッ素) N 8酸素 O 9フッ素 F アンモニア性硝酸銀水溶液にアルデヒド(RCHO)を加えて穏やかに加熱すると、アンモニア性硝酸銀水溶液中に含まれる銀イオンAg が還元されて 銀Agの単体 が生成し、鏡のようになる。 この反応を 銀鏡反応 という。#銀鏡反応 実験 反応式 #硝酸銀 #有機化学 高校化学 エンジョイケミストリープラス アルデヒドの還元性を確認する銀鏡反応の実験をしてい



化学式とは 一覧表 語呂合わせの覚え方 練習問題付き 中学理科 テラコヤプラス By Ameba




すごい アンモニア性硝酸銀水溶液 化学式 Minecraftの最高のアイデア
主な化学反応式一覧−中学理科で登場する化学反応式のまとめ yumineko / 反応の内容も詳しく書いています。全国理科教育大会実験講習 '14/8/7 写真で利用される化学反応 ① ろ紙に像を写そう(白黒写真の原理) 試薬 02mol/L硝酸銀水溶液、10mol/L 塩化ナトリウム水溶液、10mol/L チオ硫酸ナトリウム水溶液(ラベルなし)、銀に希硝酸を加える ☆銀に希硝酸を加える Ag+ HNO 3 → ★銀に希硝酸を加える 3Ag+4HNO 3 →NO+2H 2 O+3AgNO 3 銀は水素よりイオン化傾向が小さいため 2Ag+2HNO3→2 Ag(NO 3 )+H 2 ↑ × というふうにはいきません。 酸化還元反応の半反応式はAgについては、




硝酸銀 I Wikipedia



Merckmillipore Com
化学名又は一般名: 硝酸銀 Silver nitrate 別名: ― 濃度又は濃度範囲: 分子式(分子量): AgNO3() 化学特性(示性式又は構造式): CAS番号: 官報公示整理番号(化審法・安衛法): 18 分類に寄与する不純物及び 安定化添加物: ― 4.応急措置例えば,硝酸銀 AgNO 3 水溶液と塩化ナトリウム水溶液を混合すると,塩化銀 AgCl が沈殿するという反応を考えよう。まず,化学反応式は以下のようになる。 AgNO 3 + NaCl → AgCl↓ + NaNO 3化学名又は一般名 硝酸銀(I) (Silver(I) nitrate) 別名濃度又は濃度範囲 100% 分子式 (分子量) AgNO3 () 化学特性 (示性式又は構造式) CAS番号 官報公示整理番号(化審法) (1)8 官報公示整理番号(安衛法) (1)8 分類に寄与する不純物及び安定化添加物



化学式 単体 物質名 化学式 物質名 化学式 物質名 化学式 水素 マグネシウム 鉄 ヘリウム アルミニウム 銅 炭素 硫黄 亜鉛 窒素 塩素 銀 酸素 カリウム バリウム ナトリウム カルシウム 水銀 水素 H2 ヘリウム He 炭素 C 窒素 N2 酸素 O2 ナトリウム




夕凪亭別館 写真館 10 化学反応式
化学式 agno3〔硝酸銀〕 化学物質を特定できる一般的な番号 cas rn: 濃度又は濃度範囲 硝酸銀溶液 100%( 硝酸銀, ②水) ※各製品の含有量は、別表3濃度表を参照 官報公示整理番号(化審法、安衛法) (1)8〔硝酸銀〕 別表3濃度表 4.応急措置そもそも硝酸銀の半反応式はありません。 あくまで硝酸銀が酸化剤として働くときの半反応式が さっきの式になります。 半反応式では実際に反応に関与する部分しか式に書きません。それでも書きたいのなら、 AgNo3 e → Ag NO3となるのかなと思います。Fig 415 硝酸銀AgNO3 の水溶液に臭化カリウムKBr 水溶液を加えますと黄白色のAgBr の沈殿と硝酸カリ ウムKNO3 の水溶液になります。臭化銀は写真フィルムに用います。光がフィルムに当たると、臭化銀は還 元されて銀になります。 例題 44 沈殿反応の式を書く



硝酸銅




銀鏡反応 Youtube
電離式の一覧を中学生向けに作成 しました。 さっそく電離式の一覧を下に載せますが、 その下にはさらに、 電離の解説 や、 電離式の練習問題がある ので、ぜひ勉強に活用してください! 酸性の水溶液になる電離式 赤字がよく出るもの ① 塩酸の電離



2




リツキサン Burner Sur Twitter Dr Stoneのopでスタッフロールに合わせて化学構造式が描かれてたので 出てくる化合物をわかる範囲でまとめてみました 自分用に作ったものですが この画像片手にopを見てニヤニヤして貰えたら私がヨロコビます 注 原作5巻までに登場




硝酸 Wikipedia




マーカーを引いたところで Clearnote
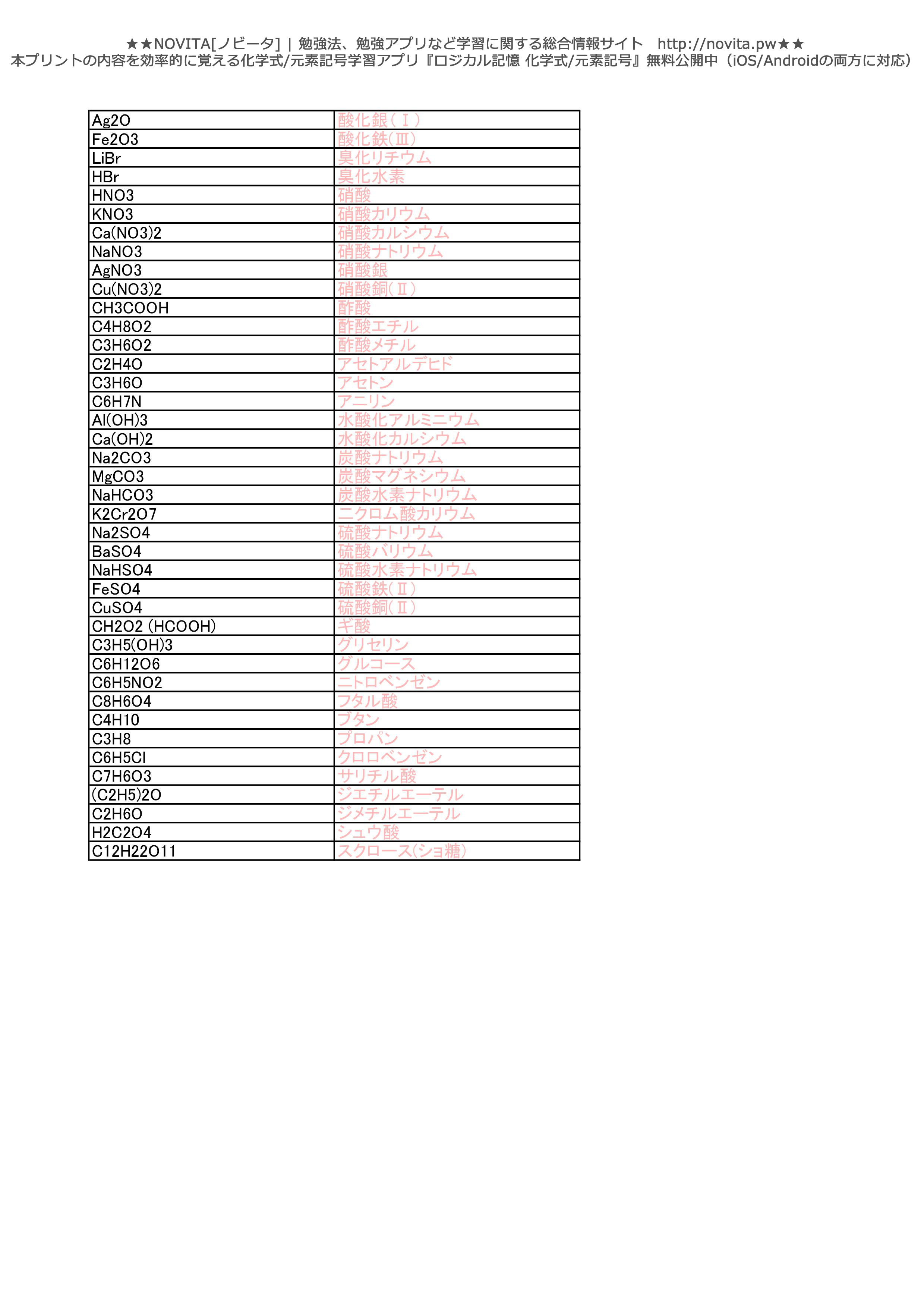



元素記号 化学式 勉強プリント Novita 勉強法



2



アセチレンとアンモニア性硝酸銀水溶液の反応式をおしえてくださ Yahoo 知恵袋
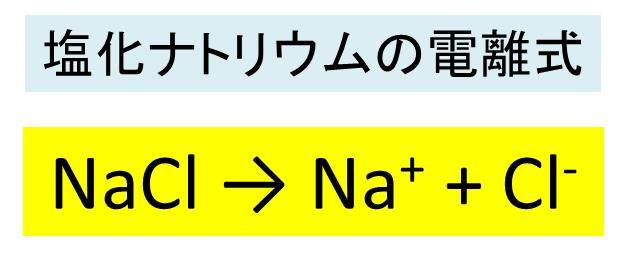



塩化ナトリウム Nacl の化学式 分子式 構造式 電子式 イオン式 分子量は 塩化ナトリウムと硝酸銀の反応式




高校有機化学 アルデヒドとケトン 銀鏡反応 フェーリング反応 ヨードホルム反応 受験の月




高校化学 アルデヒドの性質 映像授業のtry It トライイット




硝酸銀 I Wikipedia




硝酸銀 Jis Special Grade 99 8 7761 8




硝酸銀は 化学式 Agno3 と無機化合物です この化合物は写真で使用されているなど 多く他銀製品に汎用性の高い前駆体です の写真素材 画像素材 Image



化学実験 I属 銀




トレンス試薬 Wikipedia



硝酸銀 I You Iggy




実験室7 銅と硝酸銀水溶液の反応cu Agno3 Copper And Silver Ion Mts Youtube



主な化学反応式一覧 中学理科で登場する化学反応式のまとめ 教科書をわかりやすく通訳するサイト



1




高校化学 ハロゲン化銀 映像授業のtry It トライイット




食塩水に硝酸銀水溶液を加えた時の反応で 化学反応式は Nacl Agno3 N 化学 教えて Goo




高校化学 銀イオンの反応 映像授業のtry It トライイット



化学式とは 一覧表 語呂合わせの覚え方 練習問題付き 中学理科 テラコヤプラス By Ameba



化学式 単体 物質名 化学式 物質名 化学式 物質名 化学式 水素 マグネシウム 鉄 ヘリウム アルミニウム 銅 炭素 硫黄 亜鉛 窒素 塩素 銀 酸素 カリウム バリウム ナトリウム カルシウム 水銀 水素 H2 ヘリウム He 炭素 C 窒素 N2 酸素 O2 ナトリウム



硝酸銀 I You Iggy



1



Junsei Co Jp



化学式とは 一覧表 語呂合わせの覚え方 練習問題付き 中学理科 テラコヤプラス By Ameba



ある水溶液に硝酸銀水溶液を加えると 白くにごった この水溶液に Yahoo 知恵袋




化学 硝酸銀水溶液に銅を浸けると銀析出 Youtube



塩化ナトリウム Nacl の化学式 分子式 構造式 電子式 イオン式 分子量は 塩化ナトリウムと硝酸銀の反応式




指示薬まとめ 中学理科 ポイントまとめと整理




その場から一歩も動かず写真撮れ Twitter Search




高校化学基礎 イオン反応式とは 映像授業のtry It トライイット




化学 銀鏡反応が詳しく15分でわかる動画 Youtube



次の化学反応式を教えて下さい 1 鉛と硝酸銀水溶液の反応 2 銅板と Yahoo 知恵袋
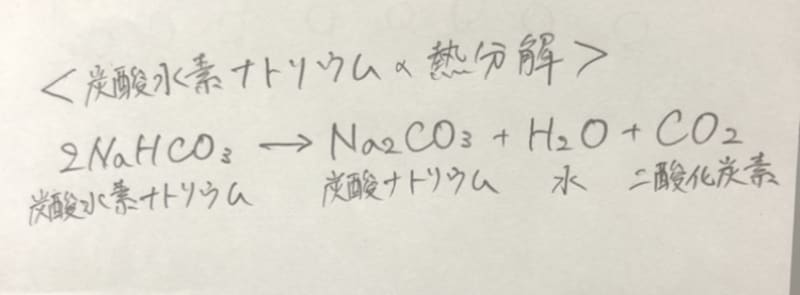



炭酸水素ナトリウムの化学反応式を教えてください アンサーズ




センター試験にでる化学反応式 数学 化学講師 佐藤学による受験生に役立つ濃縮ポイントと Etc




頻出 化学反応式 17 化学がちょっとだけ好きな社労士



Kokusan Chem Co Jp




7761 8 1mol L 硝酸銀溶液 1mol L Silver Nitrate Solution 198 詳細情報 分析 試薬 富士フイルム和光純薬




硝酸 Wikipedia
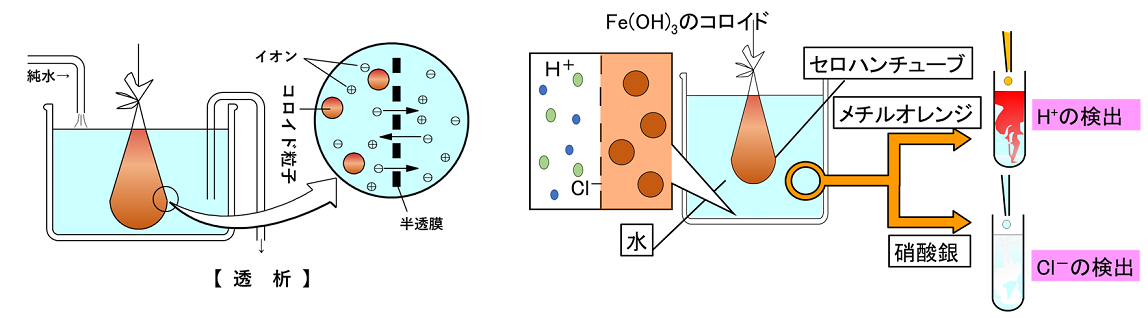



コロイド




高校理論化学 化学反応式と化学反応の量的関係 過不足のある反応 混合気体の燃焼 混合物の純度 受験の月



電位差滴定法の計算問題解答例 コンクリート診断士




化学基礎233a 化学19 04 銅 Cu は銀 Ag よりも陽イオンになりやすいので硝酸銀水溶液中では電子 E を失って銅イオン Cu2 に水溶液中の銀イオン Ag は電子を受け取って銀 Youtube



3




すごい アンモニア性硝酸銀水溶液 化学式 Minecraftの最高のアイデア



2




7761 8 0 1mol L 硝酸銀溶液 0 1mol L Silver Nitrate Solution 190 192 詳細情報 分析 試薬 富士フイルム和光純薬




硝酸銀 I Wikipedia



硝酸銀 I You Iggy



化学式 単体 物質名 化学式 物質名 化学式 物質名 化学式 水素 マグネシウム 鉄 ヘリウム アルミニウム 銅 炭素 硫黄 亜鉛 窒素 塩素 銀 酸素 カリウム バリウム ナトリウム カルシウム 水銀 水素 H2 ヘリウム He 炭素 C 窒素 N2 酸素 O2 ナトリウム




この問題ってどうやって解けばいいんですか Clearnote




水溶液に硝酸銀水溶液を加えると白色沈殿を生じる 実験から塩素が確認される理由を アンサーズ




塩化ナトリウム Nacl の化学式 分子式 構造式 電子式 イオン式 分子量は 塩化ナトリウムと硝酸銀の反応式



Updated よく出る化学式を丸暗記で覚える 大学受験必須sister化学式 元素記号 有機化合物 無機化合物 App Not Working Down White Screen Black Blank Screen Loading Problems 21




硫酸イオンと 硫酸の化学式はなぜ違うのですか 硫酸にはなぜhがつくのに 硫酸イ アンサーズ




硝酸銀の組成式なのですが なぜagno3 小さな3 Clearnote



第61章 実験 銀イオンと鉛イオン




フライング エッグ株式会社 今回の開発商品ポスターは 化学式一覧表 です Facebook



2




高校化学 Agno 水溶液の電気分解 映像授業のtry It トライイット




すごい アンモニア性硝酸銀水溶液 化学式 Minecraftの最高のアイデア



0 0mol L硝酸銀agno3水溶液50 0mlに 0 Yahoo 知恵袋




Album




50 化学式 アンモニア マインクラフトコレクション



化学式とは 一覧表 語呂合わせの覚え方 練習問題付き 中学理科 テラコヤプラス By Ameba
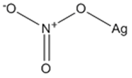



職場のあんぜんサイト 化学物質 硝酸銀 i




Album



化学反応式の問題です 塩化ナトリウム水溶液に硝酸銀水溶液を加えると Yahoo 知恵袋




製品詳細



銀滴定法によるしょう油中の食塩の定量 沈殿滴定



第16章 化学反応の量的関係



2



Quantity Of Material Ionic Reaction Formula




すごい アンモニア性硝酸銀水溶液 化学式 Minecraftの最高のアイデア




この透析後の外液に硝酸銀水溶液を加えた時に起きた化学反応のイオン反応式の作り Clearnote



よく出る化学式を丸暗記で覚える 大学受験必須sister化学式 元素記号 有機化合物 無機化合物 By 学習アプリsister Android Apps Appagg



Updated よく出る化学式を丸暗記で覚える 大学受験必須sister化学式 元素記号 有機化合物 無機化合物 App Not Working Down White Screen Black Blank Screen Loading Problems 21



銀鏡反応とフェーリング反応 原理 反応式 沈殿 色変化など 化学のグルメ




なんで沈殿するのは塩化銀ってわかるんですか 硝酸ナトリウムは違うんですか Clearnote




化学基礎 イオン反応式 Youtube




硝酸銀は 化学式 Agno3 と無機化合物です この化合物は写真で使用されているなど 多く他銀製品に汎用性の高い前駆体です の写真素材 画像素材 Image




硝酸銀溶液 林純薬工業 試薬 通販モノタロウ




5分でわかる金属樹 不思議な現象が生じる理由を理系学生ライターが徹底解説 ページ 4 4 Study Z ドラゴン桜と学ぶwebマガジン




すごい アンモニア性硝酸銀水溶液 化学式 Minecraftの最高のアイデア
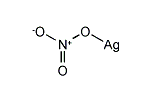



硝酸銀とは何 Weblio辞書



化学実験 I属 銀



硝酸銀の電離式を教えて下さい Yahoo 知恵袋



0 件のコメント:
コメントを投稿